Артериальная гипертензия и гиперинсулинемия – есть ли связь?
 Гиперинсулинемия или гиперинсулинемии является состояние, в котором Есть превышение уровней циркулирующего инсулина в крови. Также известный как предварительно диабет, резистентность к инсулину и синдром X, это обычно связано с поликистозом яичников (синдром поликистозных яичников) у женщин.
Гиперинсулинемия или гиперинсулинемии является состояние, в котором Есть превышение уровней циркулирующего инсулина в крови. Также известный как предварительно диабет, резистентность к инсулину и синдром X, это обычно связано с поликистозом яичников (синдром поликистозных яичников) у женщин.
Гиперинсулинемия часто принимают за диабета или гипогликемии, оба из которых являются отдельные условия.
Гиперинсулинемия может перерасти в неконтролируемый сахарный диабет, если и не лечится, и могут оставаться присутствовать при диабете происходит.
Контроль артериального давления, позволяющий эффективно улучшать прогноз ИБС у больных сахарным диабетом 2 типа, занимает сейчас приоритетное, по сути дела, первое место между другими аналогичными вмешательствами.
Известно, что контроль уровня артериального давления позволяет снизить развитие сердечно–сосудистой патологии у больных сахарным диабетом 2 типа на 51 процентов , в то время как контроль гиперлипидемии снижает показатели смертности от ИБС на 36 процентов , а тщательная коррекция уровня гликемии снижает частоту развития инфарктов миокарда на 16 процентов.
Как свидетельствуют результаты национальных профилактических программ различных стран, нормализация артериального давления, кроме того, играет ведущую роль в профилактике сахарного диабета у лиц с высоким риском его развития.
Сочетание гиперинсулинемии с артериальной гипертонией хорошо известно. Наиболее часто оно встречается у больных сахарным диабетом 2 типа и у лиц с ожирением.
Сам по себе инсулин обладает прямым сосудорасширяющим воздействием.
У нормальных людей введение физиологических доз инсулина при отсутствии гипогликемии вызывает вазодилатацию, а не повышение уровня артериального давления.
Но отмечено, что артериальное давление уменьшается при снижении дозы инсулина у больных с повышенным весом, страдающих сахарным диабетом 2 типа. Известно также, что при начале инсулинотерапии у лиц с плохо контролируемым сахарным диабетом 2 типа уровень их артериального давления нарастает.
Учитывая то, что инсулин является прямым вазодилататором, формирование артериальной гипертонии при его участии, повидимому, происходит во взаимодействии с другими физиологическими механизмами. Прежде всего это относится к взаимодействию инсулина и симпатической нервной системы.
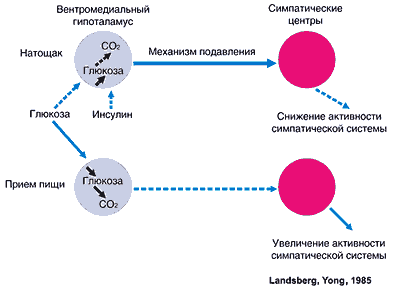
Установлено, что потребление пищи повышает, а голодание снижает активность симпатической нервной системы.
Как оказалось, инсулин играет ключевую роль во взаимосвязи потребления пищи и симпатическиобусловленной тратой энергии. После приема пищи секреция инсулина увеличивается. При этом инсулин стимулирует потребление и обмен глюкозы в регуляторных клетках, анатомически связанных с вентромедиальными ядрами гипоталамуса. Увеличение потребления глюкозы в этих нейронах ведет к уменьшению их угнетающего воздействия на ствол головного мозга. В результате расположенные там центры симпатической регуляции растормаживаются и центральная активность симпатической нервной системы (СНС) нарастает. Повышение симпатической активности после приема пищи ведет к нарастанию потребления энергетических запасов организма.
Механизм пищевой регуляции активности симпатической нервной системы позволяет экономить расход калорий в период голодания и способствует сжиганию избыточных калорий при переедании.
Ее эффект направлен на стабилизацию энергетического баланса организма и сохранение устойчивого веса тела. Ключевая роль инсулина в реализации действия этого механизма вполне очевидна.
При ожирении и диабете II типа компенсаторная гиперинсулинемия, возникающая на фоне снижения чувствительности к инсулину, ведет к значительному росту активности центральных ядер симпатической нервной системы.
И в этом случае повышенная активность симпатической нервной системы функционально направлена на увеличение уровня энергетических трат в соответствии с уровнем энергетических субстратов, имеющихся в организме. тем не менее в условиях инсулинорезистентности гиперактивизация симпатической нервной системы приводит к появлению артериальной гипертонии за счет симпатической стимуляция сердца, сосудов и почек.
Таким образом, артериальная гипертония при ожирении и диабете второго типа является своего рода нежелательным побочным продуктом действия механизмов, направленных на восстановление энергетического баланса и стабилизации веса тела.
Результаты экспериментальных исследований подтвердили: острое и хроническое повышение концентрации инсулина в крови стимулирует активность симпатической нервной системы и повышает концентрацию катехоламинов в крови.
Дополнительные доказательства, подтверждающие стимулирующий эффект инсулина на симпатическую активность, получены при испытаниях соматостатина.
Этот гормон, угнетающий эндогенную секрецию инсулина, приводит к снижению концентраций норадреналина в плазме и уменьшению уровня артериального давления у больных с гиперинсулинемией. При нефармакологических воздействиях, уменьшающих проявления инсулинорезистентности (ограничение калорий, снижение веса, физические упражнения), также обнаружено параллельное снижение концентрации инсулина в крови, активности симпатической нервной системы и уровня артериального давления.
Данные эпидемиологических исследований подтвердили значимость гиперинсулинемии и активации симпатической нервной системы в формировании артериальной гипертонии на популяционном уровне. В Normative Aging Study, проведенном в Бостоне, США, у участников исследования активность симпатической нервной системы оценивалась по уровню суточной экскреции норадреналина с мочой. Было обнаружено, что эта активность прямо коррелирует с индексом массы тела и достоверно повышена у лиц с гиперинсулинемией. Стимулирующий эффект инсулина в отношении симпатической нервной системы при гиперинсулинемии не отличается от такового у лиц с нормальной чувствительностью к инсулину.
 Результаты исследования свидетельствуют о том, что инсулин и инсулинорезистентность являются физиологическими компонентами системы регуляции артериального давления и ведущую роль в реализации их воздействия на уровень артериального давления играет сопутствующая активизация симпатической нервной системы.
Результаты исследования свидетельствуют о том, что инсулин и инсулинорезистентность являются физиологическими компонентами системы регуляции артериального давления и ведущую роль в реализации их воздействия на уровень артериального давления играет сопутствующая активизация симпатической нервной системы.
Активации центральных отделов СНС изменяет обмен норадреналина в периферических окончаниях СНС. Во многих физиологических ситуациях периферическая симпатическая нервная система реагирует не как единое целое, а как сочетание отдельных частей, имеющих выраженные региональные отличия по степени развивающейся симпатической активации.
Измерения регионального выделения норадреналина позволили сделать вывод о том, что в условиях гиперинсулинемии и инсулинорезистентности при ожирении активность периферической симпатической нервной системы значительно повышена в почках и снижена в сердце. При этом уровень симпатической активности в скелетной мускулатуре тем выше, чем больше вес тела, индекс массы тела и процент жира в организме. Почечная гиперсимпатикотония усиливает задержку натрия, жидкости, изменяет почечную гемодинамику, увеличивает выделение ренина, приводя в результате к повышению артериального давления.
Особая роль почек в развитии инсулининдуцированной артериальной гипертонии была осознана совсем недавно. Результаты исследований показали, что двусторонняя деинервация почек у крыс предотвращает быстрый подъем артериального давления во время инфузии инсулина и эффективно снижает сформировавшуюся гипертонию, индуцированную длительным введением инсулина. Деинервация почек снижает выраженность гипертонии и у собак с ожирением и гиперинсулинемией. Эти экспериментальные данные свидетельствуют о том, что наличие интактной симпатической почечной иннервации является обязательным условием развития артериальной гипертонии, связанной с устойчивой гиперинсулинемией.
Нервы почек играют важнейшую роль в контроле почечных функций. Хорошо известно, что почечная регуляция баланса жидкости и натрия играет решающую роль в долгосрочном контроле артериального давления в норме и при патологии.
Cтимуляция эфферентных (центробежных) нервов почек изменяет гемодинамику почек, увеличивает канальцевую реабсорбцию натрия.
Совсем недавно было обнаружено, что при сахарном диабете 2 типа существует еще один механизм, приводящий к усилению почечной гиперсимпатикотонии. Он связанс влиянием гипергликемии на экспрессию гена ангиотензиногена в почечной ткани в условиях инсулинорезистентности.
В норме инсулин подавляет стимулирующий эффект гипергликемии на экспрессию гена ангиотензиногена в клетках проксимальных канальцев почек и препятствует увеличению секреции ангиотензиногена. При сахарном диабете 2 типа в связи с наличием инсулинорезистентности подавление инсулином глюкозостимулируемой экспрессии гена ангиотензиногена в клетках проксимальных канальцев почек не происходит, экспрессия гена растормаживается и секреция ангиотензиногена усиливается. Повидимому, именно этот механизм лежит в основе обнаруженного увеличения продукции ангиотензина II в клубочковых и канальцевых клетках почечной ткани под влиянием гипергликемии.
 Внутрипочечный ангиотензин II связывается с многочисленными ангиотензин I рецепторами клубочков и канальцев почек, с рецепторами ее сосудистой сети и клеток интерстиция. Значительное увеличение количества АТ1 рецепторов отмечено при сахарном диабете 2 типа.
Внутрипочечный ангиотензин II связывается с многочисленными ангиотензин I рецепторами клубочков и канальцев почек, с рецепторами ее сосудистой сети и клеток интерстиция. Значительное увеличение количества АТ1 рецепторов отмечено при сахарном диабете 2 типа.
Воздействие ангиотензина II на рецепторы АТ1, контролирующие выделение норадреналина в синапсах симпатической нервной системы почек, ведет к нарастанию ренальной гиперсимпатикотонии.
Таким образом ренальная гиперсимпатикотония, являясь характерной особенностью инсулин–индуцированной артериальной, возникает, во–первых, как последствие гиперинсулинемической стимуляции центральных механизмов симпатической нервной системы и во–вторых, как результат увеличения выделения норадреналина в симпатических синапсах почек вследствие активизация почечной тканевой ренин–ангиотензиновой системы в условиях инсулинорезистентности.
Гиперсимпатикотония усиливает секрецию ренина в почках. Повышение ренина активизирует ренинангиотензинальдостероновую систему (РААС). Многие авторы отмечают повышение активности ренинангиотензиновой системы при компенсированном сахарном диабете.
Увеличение концентрации ангиотензина II воздействует на рецепторы резистивных сосудов и на АТ1рецепторы в нейромышечных синапсов скелетной мускулатуры. В результате возникает подъем артериального давления и дальнейшее нарастание симпатикотонии в скелетной мускулатуре. Длительное повышение мышечной симпатической активности вызывает уменьшение капиллярной сети мышц, снижает количество медленно сокращающихся мышечных волокон, определяющих уровень чувствительности организма к инсулину. Ухудшение кровотока скелетных мышц, являющихся главным потребителем глюкозы в организме, приводит к понижению транспорта глюкозы в мышцах и дальнейшему нарастанию показателей инсулинорезистентности и компенсаторной гиперинсулинемии. Формируется порочный круг, ведущий к возобновляющейся активации всех входящих в него компонентов.
Приведенные выше данные о роли начальной активации симпатической нервной системы и последующей активации ренинангиотензиновой системы в развитии артериальной гипертонии у больных сахарным диабетом 2 типа вполне объясняют причину получения таких результатов.
Снижение симпатической активности является важнейшей задачей профилактики сердечно–сосудистых осложнений у больных сахарным диабетом 2 типа. Препараты, которые способны не только блокировать эту активность, но и воздействовать на ключевые механизмы, ее запускающие и поддерживающие, несомненно, обладают большим потенциалом при инсулин–индуцированной артериальной гипертонии и достойны того пристального внимания со стороны клиницистов, которое отмечается сегодня. Так появился аюрведический препарат Зенслим Кардио.






Как влияет высокий уровень инсулина на кровяное давление?
Как влияет высокий уровень инсулина на кровяное давление?
Как известно, риск сердечных заболеваний связан с повышенным артериальным давлением. Оно может быть обусловлено многими причинами, в том числе и высоким уровнем инсулина.
1. Инсулин способствует задержке соли в организме, а это ведет к удержанию жидкости. А высокое содержание жидкости в организме поднимает давление.
2. Инсулин оказывает возбуждающее воздействие на нервную систему, что ведет к увеличению объема крови, выкачиваемой в артерии с каждым сердечным сокращением. Это не только повышает кровяное давление, но и приводит к отвердению артериальных стенок и потере ими гибкости, что может вызвать повреждение сердечных тканей, сердечный приступ и даже привести к внезапной смерти.
Какие бывают симптомы гиперинсулинемии?
Какие бывают симптомы гиперинсулинемии?
Определить симптомы гиперинсулинемии бывает порой очень непросто. На начальном этапе для нее характерна скрытая форма. И все же у большинства пациентов отмечаются схожие симптомы:
Особенности патогенеза артериальной гипертензии у больных с мета
Особенности патогенеза артериальной гипертензии у больных с метаболическим синдромом
Резюме
Изучение особенностей патогенеза артериальной гипертензии (АГ) у пациентов с заболеваниями, входящими в понятие метаболического синдрома (МС), представляет не только теоретический интерес, но и имеет большое практическое значение. Установлено, что у лиц с туловищным ожирением АГ является наиболее часто встречаемым компонентом МС и возникает значительно раньше, чем выявляются нарушения липидного и углеводного метаболизма. Проведенные исследования показали, что больные с туловищным ожирением имеют существенные изменения со стороны гипоталамо-гипофизарно-надпочечниковой оси, способствующие не только появлению столь характерного типа ожирения, но и принимающие непосредственное участие
в развитии АГ. Установлено, что помимо нарушений центральных механизмов регуляции, симпатикотонии, инсулинорезистентности и гиперинсулинемии в развитии АГ у больных туловищным ожирением немаловажное значение имеет функциональное состояние жировой ткани. Нарушения с ее стороны и развитие вследствие этого адипозопатии могут в ряде случаев стать первопричиной всего каскада МС. При этом дисфункция адипоцитов может носить как генетически обусловленный, так и приобретенный характер. Расшифровка причин и механизмов развития АГ у пациентов с МС представляет особый интерес, так как позволит более целенаправленно решать вопросы профилактики и лечения этого заболевания.
Ключевые слова: артериальная гипертензия, метаболический сердечно-сосудистый синдром, инсулинорезистентнось, гиперинсулинемия, гиперкортизолизм, адипозопатия.
Сведения об авторах
Красильникова Елена Ивановна – д-р мед. наук, проф. каф. факультетской терапии СПбГМУ им. акад. И.П.Павлова Минздравсоцразвития РФ, вед. науч. сотр. ФЦСКЭ им. В.А.Алмазова Минздравсоцразвития РФ, Санкт-Петербург.
E-mail: [email protected]
Баранова Елена Ивановна – д-р мед. наук, проф. каф. факультетской терапии с курсом эндокринологии Санкт-Петербургского
ГМУ им. акад. И.П.Павлова, вед. науч. сотр. Федерального центра сердца, крови и эндокринологии им. В.А.Алмазова
Благосклонная Янина Владимировна – д-р мед. наук, проф. вед. науч. сотр. Федерального центра сердца, крови и эндокринологии
им. В.А.Алмазова
Изучение механизмов развития артериальной гипертензии (АГ) у различных когорт больных имеет большое практическое значение, так как позволяет выработать наиболее эффективную, патогенетически направленную тактику лечения. Согласно большим эпидемиологическим исследованиям, проведенным за последние годы, изолированное развитие АГ встречается чрезвычайно редко. Установлено, что у 30–75% больных гипертонической болезнью (ГБ) имеется ожирение или избыточный вес, несколько реже (18–50%) выявляются в различной степени выраженные нарушения углеводного метаболизма, а при проведении специальных исследований до 60% больных АГ имеют нарушения липидного спектра крови [28, 30, 33, 37, 38, 40–44, 47, 50, 52, 55, 56]. При этом подчеркивается, что избыточный вес или ожирение , как правило, хронологически предшествуют развитию ГБ [1–3, 5, 6, 27].
В результате проведенных нами исследований установлено, что у 4880 больных, имевших заболевания, входящие в понятие метаболического сердечно-сосудистого синдрома (МС), наиболее ранним клиническим проявлением МС было ожирение, АГ, как правило, возникала в более позднем возрасте на фоне предшествующего ожирения. Клинические проявления ишемической болезни сердца (ИБС) возникали у большинства обследованных больных позднее, с пиком развития в возрасте 50–59 лет. Наиболее поздним компонентом МС являлся сахарный диабет (СД) типа 2, который, как правило, диагностировался после 40 лет, при этом его частота с возрастом нарастала (рис. 1).
Полученные данные позволяют предположить наличие тесных патогенетических связей между ожирением и АГ [1, 2]. Именно факт частого сочетания ожирения и АГ послужил поводом для внесения предложения, поддержанного многими учеными, считать, что первой ступенью развития МС является не только туловищное ожирение, но и тесно связанная с ним АГ, что подчеркивает общность патогенеза этих заболеваний. Высказанные позиции основываются на результатах многочисленных исследований, свидетельствующих о том, что у больных с полным МС АГ встречается почти в 100% случаев, тогда как частота развития других компонентов МС – гипертриглицеридемия, снижение содержания липопротеинов высокой плотности (ЛПВП) в сыворотке крови, а также нарушения углеводного гомеостаза – может значительно варьировать. Однако, не вступая в полемику относительно совершенства классификации МС, следует заключить, что, безусловно, существуют определенные особенности патогенеза АГ у лиц с туловищным ожирением, изучение которых представляет не только теоретический интерес, но и имеет существенное практическое значение [1, 11–13, 15, 16, 18].
Учитывая имеющиеся данные о чрезвычайно частом сочетании туловищного ожирения и АГ, можно предположить, что ряд патогенетических звеньев развития этих заболеваний являются общими, т.е. не только само ожирение, но и факторы, участвующие в его развитии, могут оказывать влияние на уровень АД. Что касается причин развития ожирения, то необходимо признать, что несмотря на большое количество проведенных исследований вопрос остается открытым. Не вызывает сомнения, что основной причиной возникновения избыточной массы тела являются нарушения пищевого поведения, ведущие к хроническому перееданию, что может быть следствием как изменения центральных механизмов регуляции (кора головного мозга, гипоталамус, центр аппетита, зрительный, обонятельный, вкусовой анализаторы), так и возникать в результате первичных особенностей функционирования висцеральной жировой ткани (в ряде случаев имеющих генетически обусловленную природу). При этом большое значение имеет физический термогенез (рис. 2) [7, 8, 21, 22, 24, 32, 57, 58].
Доказательством наличия тесных взаимосвязей между центральными механизмами регуляции и жировой тканью являются полученные нами данные, свидетельствующие о наличии у больных с туловищным типом ожирения снижения чувствительности гипоталамо-гипофизарно-надпочечниковой оси к действию кортизола, что ведет к небольшому, но все же хроническому избытку секреции кортизола [7]. Установлено, что у больных с туловищным ожирением имеется достоверное увеличение суточной экскреции 17-гидроксикортикостероидов
(17-HOCS) – метаболитов кортизола – не только по сравнению с лицами контрольной группы, но и с больными с глютеофеморальным типом ожирения (рис. 3).
Кроме того, чрезвычайно важным представляется факт отсутствия подавления экскреции 17-HOCS у больных с туловищным ожирением под влиянием 0,5 мг дексаметазона, в то время как у лиц контрольной группы и больных с глютеофеморальным ожирением даже такие малые дозы дексаметазона вызывали резкое угнетение синтеза адренокортикотропного гормона и, соответственно, экскреции метаболитов кортизола (см. рис. 3).
Известно, что кортизол стимулирует гормонозависимую липопротеиновую липазу (ЛПЛ) на капиллярах жировых клеток верхней половины туловища, брюшной стенки и висцерального жира (кортизолзависимая жировая ткань). В случае хронического избытка кортизола происходит активация ЛПЛ, в результате усиливается распад триглицеридов (ТГ), входящих в состав липопротеинов низкой и очень низкой плотности (ЛПНП, ЛПОНП), а в постпрандиальный период – и в хиломикроны (ХМ) и ремнанты ХМ; в результате этого высвобождаются жирные кислоты (ЖК), поступление которых в адипоциты приводит к повышенному синтезу нейтрального жира, развитию гипертрофии жировых клеток и столь характерного туловищного ожирения (рис. 4).
Роль кортизола в развитии туловищного ожирения подтверждает и характерное для него распределение жира, напоминающее синдром Кушинга. Не вызывает сомнения, что фенотипическая схожесть пациентов с туловищным ожирением и синдромом Кушинга не может быть случайной, особенно учитывая, что при обоих заболеваниях у большинства пациентов имеется АГ, атерогенная дислипидемия и в различной степени выраженные нарушения углеводного обмена. Что касается роли избытка кортизола в механизмах развития АГ, то существует огромное количество работ, посвященных этому вопросу, подробно изучено более 20 эффектов этого гормона, способствующих повышению артериального давления (АД). Не исключается, что у ряда пациентов в основе гиперпродукции кортизола может лежать и генетическая предрасположенность [19, 22, 25]. Таким образом, полученные нами данные не только расширяют имеющиеся представления о патогенезе туловищного типа ожирения, но и доказывают существенную роль кортизола в механизмах развития всего каскада МС.
В последние годы установлено, что помимо роли центральных механизмов в регуляции массы тела и уровня АД висцеральные адипоциты являются чрезвычайно активными в метаболическом плане и секретируют большое количество адипоцитокинов, которые так же могут не только регулировать пищевое поведение человека, но и оказывать существенное влияние на чувствительность тканей к инсулину, показатели липидного спектра крови, процессы воспаления, тромбогенеза, функциональную активность эндотелия, повышать активность симпатической нервной системы (СНС), а также оказывать влияние на уровень АД [9, 11, 14, 22]. Поэтому вопрос, является ли инсулинорезистентность первопричиной всего каскада МС или следствием туловищного ожирения наряду с другими метаболическими расстройствами, остается открытым. Однако в любом случае роль активации СНС, имеющейся у больных с туловищным ожирением, в нарастании инсулинорезистентности и гиперинсулинемии с одной стороны и развитии АГ с другой – не вызывает сомнения (рис. 5).
Роль инсулина в регуляции АД в норме хорошо изучена [22, 19]. В условиях гиперинсулинемии помимо прямого влияния на тонус гладких мышц сосудов и активность
b-адренорецепторов сосудистой стенки, избыток инсулина, способствует повышению активности симпатоадреналовой и ренин-ангиотензиновой систем, усиливает реабсорбцию натрия и воды в почках, что в конечном итоге способствует развитию АГ (рис. 6) [54]. Однако многие механизмы возникновения симпатикотонии, обусловленной инсулинорезистентностью/гиперинсулинемией, до сих пор остаются невыясненными.
Предполагается, что инсулин стимулирует захват глюкозы нейронами вентромедиальных ядер гипоталамуса, что изменяет функциональное состояние нейронов и уменьшает их тормозное влияние на активные центры СНС в стволе мозга. Кроме того, инсулин тормозит освобождение и усиливает захват норадреналина нервными окончаниями. Некоторые исследователи не исключают, что повышенный ответ СНС на стимуляцию инсулином может быть генетически детерминирован. Определенное значение в развитии АГ имеет стимулирующее влияние инсулина на синтез коллагена, процессы гипертрофии и пролиферации гладкомышечных клеток и фибробластов сосудистой стенки [51]. Так, в проведенных нами исследованиях установлено, что толщина комплекса интима–медиа сонной артерии и количество циркулирующих в крови десквамированных эндотелиоцитов у больных с МС тесно коррелируют с повышенным уровнем инсулина и атерогенных фракций липопротеинов [3]. Характерное для лиц с инсулинорезистентностью и гиперинсулинемией уменьшение ответа на вазодилататорное и усиление на вазоконстрикторное воздействие может быть обусловлено не только изменениями метаболизма и архитектоники сосудистой стенки, но также влияниями на эндотелий сосудов и тромбоциты, сопровождающимися усилением продукции эндотелина, тромбоксана А2, простагландина F2 и уменьшением синтеза простациклина. Немаловажное значение в изменениях функционирования эндотелия может принадлежать и характерному для таких больных усилению процессов перекисного окисления [31, 34, 46].
В определенной мере роль инсулина в генезе АГ подтверждена в проведенных нами исследованиях, касающихся больных СД типа 1, в лечении которых в течение длительного времени использовались нефизиологические, большие дозы инсулина. У этих пациентов, имевших хроническую передозировку экзогенного инсулина, частота АГ превышала таковую у сопоставимой группы больных, получавших физиологические дозы инсулина, почти в 6 раз [3]. Однако, несмотря на проведенные исследования, в отношении причинно-следственных взаимосвязей гиперинсулинемии и АГ многое остается неясным. Так, в целом ряде исследований указывается на возможности наличия общего, генетически детерминированного дефекта, обусловливающего как инсулинорезистентность, так и АГ. Установлено, что у больных АГ и гиперинсулинемией имеется значительное увеличение содержания натрия в эритроцитах и снижение их осмотической резистентности. В ряде исследований выявлены изменения в соотношении медленно сокращающихся и быстро сокращающихся миофибрилл скелетных мышц в пользу увеличения последних. В то время как известно, что для быстро сокращающихся миофибрилл характерны более высокий гликолиз и относительная резистентность к инсулину [49]. В случае хронического избытка инсулина содержание натрия в крови и непосредственно в сосудистой стенке возрастает, что повышает ее чувствительность к прессорным агентам [54].
Помимо роли избытка инсулина в активации СНС в последние годы все большее внимание стало уделяться лептину – гормону, выделяемому висцеральными адипоцитами. Установлено, что для больных с туловищным ожирением характерно развитие гиперлептинемии и лептинорезистентности (аналогично инсулинорезистентности), приводящей к повышению тонуса СНС и АД. Определенное значение в повышении АД придается другому хорошо изученному гормону жировой ткани – адипонектину. Известно, что адипонектин способствует повышению чувствительности тканей к инсулину и таким образом обладает гипогликемизирующим действием, понижает уровень атерогенных фракций в сыворотке крови и способствует снижению АД. В связи с этим недостаток выработки адипонектина, свойственный больным с туловищным ожирением, может принимать непосредственное участие в развитии у них АГ [17, 24, 26, 29, 45, 53].
Таким образом, патогенез АГ у больных с туловищным ожирением и МС имеет целый ряд особенностей, которые необходимо учитывать при выборе лечебной тактики. Необходимо понимать, что активация СНС может выступать в ряде случаев в качестве первопричины развития всего каскада МС, так как известна роль стресса в механизмах развития ожирения. В этом случае инсулинорезистентность, гиперинсулинемия и нарушения адипостата являются вторичными по отношению к гипертонусу СНС (рис. 7).
Как известно, реализация эффектов СНС опосредована катехоламинами – норадреналином и адреналином, функционирующими как нейромедиаторы центральной нервной системы и активно участвующими практически во всех обменных процессах, происходящих в организме. Эффекты катехоламинов реализуются через специфические рецепторы. В настоящее время описаны 5 групп адренорецепторов, которые различаются по локализации и эффектам, это a1-, a2-, b1-, b2-, b3-адренорецепторы. Установлено, что активация адренорецепторов происходит посредством G-белков и циклического аденозинмонофосфата (цАМФ).
Так, связывание a-субъединицы G-белка с b1- и b2-адренорецепторами приводит к повышению внутриклеточной концентрации цАМФ, что, в свою очередь, вызывает сокращение миокарда, расслабление мускулатуры сосудов, бронхов, активацию гликогенолиза и повышение секреции инсулина [4, 10]. b3-адренорецепторы привлекают особое внимание исследователей в плане изучения роли СНС в развитии ожирения. Известно, что эти рецепторы расположены, главным образом, в адипоцитах, причем преимущественно бурой жировой ткани. Стимуляция этих рецепторов ведет к усилению липолиза и термогенеза в адипоцитах, повышению теплопродукции, связанной с распадом жира в клетках бурой жировой ткани. В свою очередь, увеличение поступления в кровь свободных ЖК способствует развитию инсулинорезистентности, гиперинсулинемии и прогрессированию ожирения [4, 10, 21, 35, 36, 39, 48]. В последующем именно эти механизмы могут способствовать развитию хронической симпатикотонии, изменению суточного профиля АД и развитию поражения органов-мишеней. Безусловным доказательством вышесказанного являются результаты проведенного нами в 1999 г. пилотного исследования с использованием в лечении больных с избыточным весом, нарушением толерантности к глюкозе и ГБ моксонидина (Физиотенз, Abbott Products), препаратом сравнения являлся метформин [17]. Было установлено, что под влиянием моксонидина наблюдались не только нормализация цифр АД, но и достоверное снижение уровня глюкозы и инсулина плазмы крови при проведении пациентам глюкозотолерантного теста. Факт улучшения чувствительности тканей к инсулину и снижения его уровня в крови, выявленный нами в ходе исследования, представлялся чрезвычайно важным, поскольку роль гиперинсулинемии в механизмах развития ожирения, АГ, дислипидемии и прогрессировании всего симптомокомплекса МС хорошо известна [20, 35, 36, 54]. Обращало внимание наличие у Физиотенза не только самостоятельного сахаропонижающего эффекта, но и его способность достоверно снижать массу тела. При этом в плане влияния на такие показатели, как индекс чувствительности к инсулину и масса тела, влияние моксонидина было сопоставимым с эффектами метформина. В дальнейшем полученные данные были подтверждены в многоцентровом исследовании ALMAZ.
Таким образом, приведенные данные свидетельствуют о существенной роли симпатикотонии в развитии ожирения, инсулинорезистентности, гиперинсулинемии, АГ, а в дальнейшем и всего каскада МС. В связи с вышесказанным можно полагать, что препараты, способствующие устранению симпатикотонии, особенно при их использовании на ранних стадиях, будут способствовать предотвращению развития заболеваний, входящих в понятие МС (рис. 8).
источник: http://www.consilium-medicum.com/article/21548
Чем опасна гиперинсулинемия
Чем опасна гиперинсулинемия
Итак, «режим кафетерия» приводит к тому, что примерно через каждый час в крови нарастает последовательно уровень глюкозы, а за ним и инсулина, опять-таки с интервалом час-полтора. Однако функции инсулина вовсе не исчерпываются только отправкой глюкозы в клетки мыщц и жировой ткани. И накачав, например, мышечные клетки глюкозой, инсулин и дальше отслеживает их судьбу уже внутри клеток (через так называемых вторичных посредников, которые действуют уже внутри клеток).
И в самом деле, что делать, если глюкоза не «сгорела» полностью, например, вследствие недостаточной мышечной нагрузки (а такое в наше время не редкость!)? Тогда ее надо отправить на более длительное хранение. И вот здесь возможны два варианта. Или глюкоза будет упакована в виде полимера гликогена, из которого по мере необходимости можно будет вновь получить глюкозу, или глюкоза будет преобразована (уже необратимо!) в жиры. Последний процесс носит название липогенез (синтез жиров), и при ежечасном поступлении еды (собственно, «режим кафетерия»!), это ведет к избыточному синтезу жиров из углеводов, к чему и сводится данный эффект гиперинсулинемии. Собственно говоря, мы в одном шаге от уже почти неизбежного ожирения.
А что происходит дальше - уже более или менее известно. Ожирение ведет к прогрессирующему снижению чувствительности тканей к инсулину - так называемой инсулинорезистентности - и вот мы уже в одном шаге от сахарного диабета второго типа, заболевания, которое в современном цивилизованном мире приобретает характер пандемии.
Далее, повышенный синтез жиров ведет к увеличению содержания в крови так называемых липопротеинов очень низкой плотности - жиробелковых частиц крови с повышенным содержанием жировой компоненты - одного из главных факторов риска начальных стадий атеросклероза, еще одной «болезни цивилизации». Список заболеваний, связанных с ожирением можно было бы продолжить, но, думаю, и этого более чем достаточно.
«Будьте здрасти!» - получите тот самый «метаболический синдром»! Он же "синдром Х", он же “смертельный квартет”, он же «синдром инсулинорезистентности», он же «смертельный секстет»!
источник: http://gerontology-explorer.ru/9e09f251-9c17-41ab-abe4-2710388bcbef.html